Tilpassing, Effektivitet & Kostnadsfordel
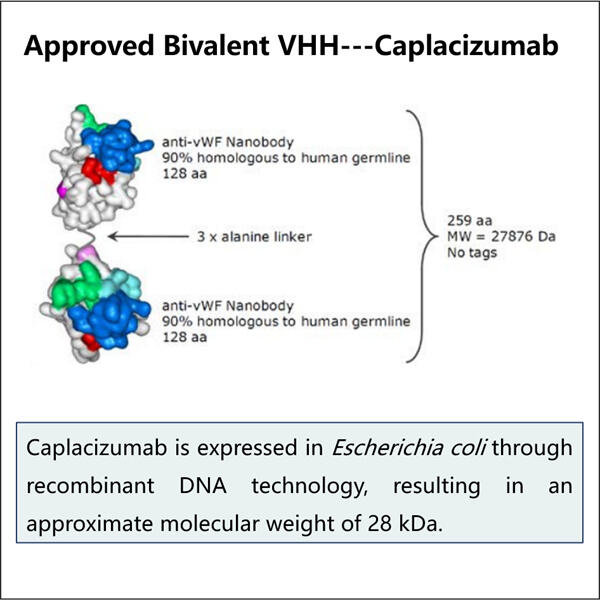
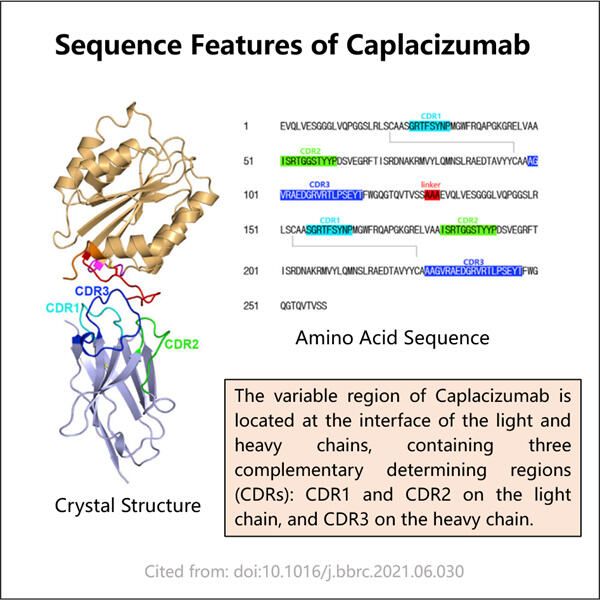
Yaohai Bio-Pharma har erfaring med å produsere biologiske stoffer som er laget av mikroorganismer. Vi tilbyr skreddersyede RD-løsninger og produksjonstjenester samtidig som vi minimerer potensielle risikoer. Vi har jobbet med ulike teknikker, såsom rekombinante cellulære subenheter, vaksiner (inkludert peptider), vekstfaktorer, hormoner og Caplacizumab-produksjon. Vi er spesialister i mange mikroorganismer, som gjerme ekstracellulær og intracellulær sekresjon (oppgitt opp til 15g/L) og bakteriell intracellulær løselighet og inklusjonslegemer (oppgitt opp til 10g/L). Vi har også utviklet en BSL-2-fermentasjonsplattform for å lage bakterielle vaksiner. Vi har en sporrekord for å forbedre produksjonsprosesser, dermed øke avkastning og redusere kostnader. Vi har et høytt effektivt teknisk team for å sikre puntuell og kvalitetsmessig leveranse av prosjekter. Dette hjelper oss å få dine unike produkter raskere på markedet.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN