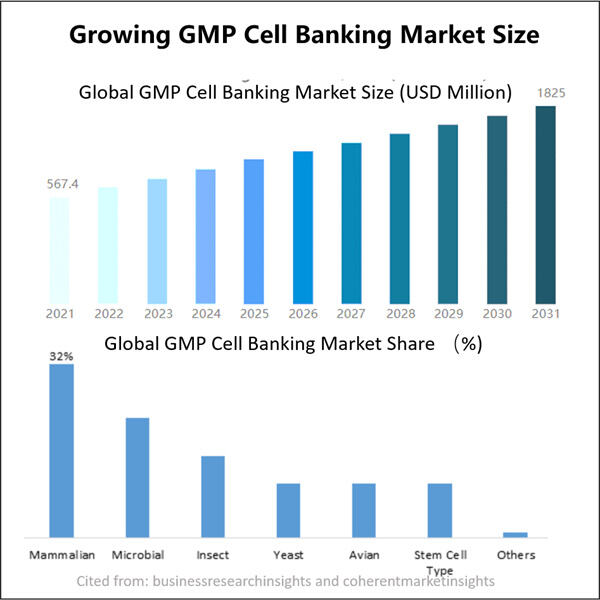
Fordelene ved GMP-mikrobiell cellebank for biofarmasøytisk utvikling
Hva vinner jeg ved å bruke GMP Mikrobiell Cellebank og sette den inn i produksjonen av mitt legemiddel? Dette vil effektivt spare noe produksjons tid, som er en av de nøkkel fordeler, siden det kan bekrefte om cellene er konsistente over flere produksjoner. Dette tilsvarer konsistent cellekvalitet, batch etter batch innen samme batteri. Kvalitetskontroll - er viktig slik at behandlingen faktisk følger deg trygt hjem. Med en cellebank klar, kan produsenter av medisiner lage en ny batch nesten så snart de blir kort på den siste. Dette er for å sikre at det er en god og regelmessig forsyning av medisin.
Selskapet må sikre en patentert prosedyre og oppbevare sine celler i en GMP CMV Antigen Produksjon . Disse cellene som trengs for å lage medisiner må beskyttes mot tannkjøttinflammering og andre forurensetninger. Dette betyr at ting som celler vokser i et rent og sterilt område. Dette betyr også at deres miljø er rent og fritt fra eventuelle kontaminanter, ikke sant? Cellene blir kryopreservert til transport og bevaring ved meget lave temperaturer. Cellebanken må også sørge for at ingenting dårlig (som bakterier eller virus som kan være farlig) kommer inn i dem under bevarelse. Å ta sådan en varemeans å sikre at cellene er både rene og klare til bruk.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN