Testreszabás, Hatékonyság & Költséghatékonyság
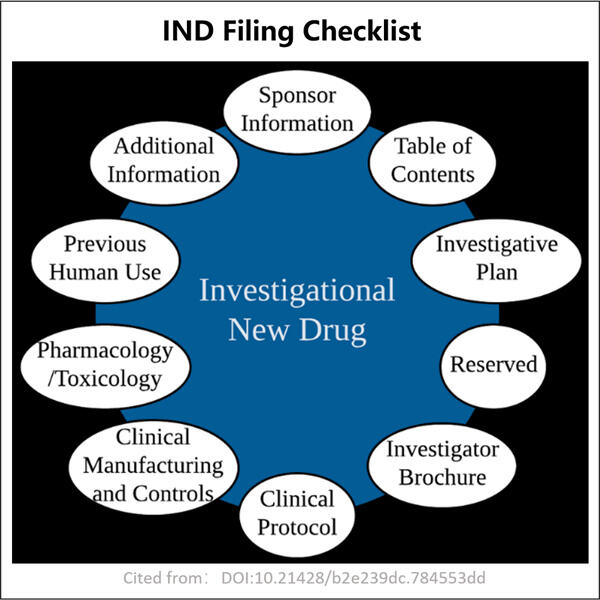
A Yaohai Bio-Pharma tapasztalatban részes az élelmiszermikrobiális forrású biológiák fejlesztésében. Személyre szabott kutatási és fejlesztési (RD) megoldásokat, valamint gyártási szolgáltatásokat kínálunk, miközben biztosítjuk, hogy nincsenek kockázatok. Különböző területeken dolgoztunk, például a reziduumban alapuló rekombináns oltásokon, az IND és BLA Kitöltési Ellenőrzési Listán, citokinokon, növekedési faktorokon, egyedülálló tartományú antigéneken, enzimeken, plazmid DNA-n, mRNA-n és másokon. Szakértők vagyunk sokféle mikroorganizmus terén, beleértve a toraszt extraceluláris és intraceluláris sécretiót (legfeljebb 15g/L teljesítmény) valamint a baktériumok intraceluláris oldható anyagokat és inklúziós testet (legfeljebb 10g/L teljesítmény). Fejlesztettük ki a BSL-2 fermentációs platformot a baktérium-alapú oltások létrehozására. Megmutattuk, hogy javíthatjuk a termelési folyamatokat, így növeljük a teljesítményt és csökkentjük a költségeket. Nagyon hatékony technológiai csapatunkkal időpontosan és minőségesen teszünk projektet, és gyorsabban hozzuk piacra a termékeidet.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN