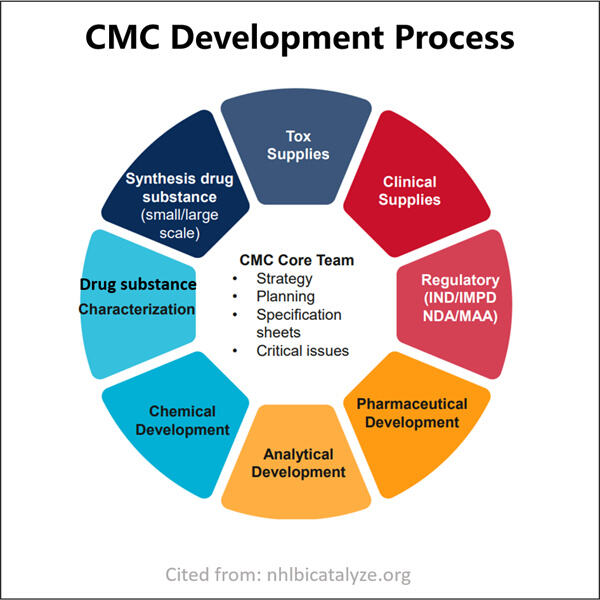
Expertise professionnelle et expérience approfondie
Yaohai Bio-Pharma est un CDMO de premier plan dans le domaine des biologiques microbiens. Notre principale activité se concentre sur la production de la section CMC dans les demandes d'autorisation de médicaments et sur les thérapies pour soigner les animaux de compagnie, la santé humaine et vétérinaire. Nous disposons de plates-formes RD ultramodernes et de technologies de fabrication couvrant l'ensemble du processus de fabrication, depuis le développement de souches microbiennes, la banque cellulaire, le développement de procédés et de méthodes, jusqu'à la fabrication clinique et commerciale, garantissant ainsi la livraison réussie de solutions innovantes. Avec le temps, nous avons acquis une vaste expertise en bio-traitement à base de micro-organismes. Nous avons réussi plus de 200 projets mondiaux et aidons nos clients à naviguer dans les règles et réglementations de l'US FDA, de l'UE EMA, de l'Australie TGA et de la Chine NMPA. Grâce à notre expérience et à notre expertise, nous sommes en mesure de répondre rapidement aux exigences du marché et d'offrir des services CDMO sur mesure.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN