Độ Tuỳ Chỉnh, Hiệu Quả & Tiết Kiệm Chi Phí
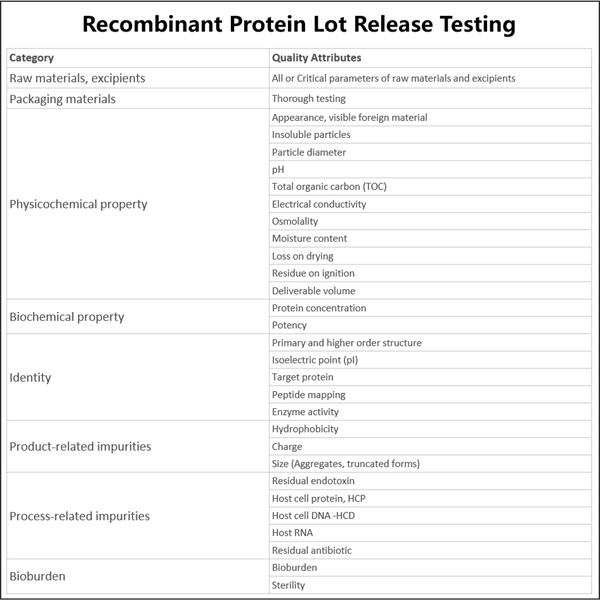
Yaohai Bio-Pharma có kinh nghiệm trong việc sản xuất sinh học được tạo ra từ vi sinh vật. Chúng tôi cung cấp các giải pháp R&D tùy chỉnh cũng như dịch vụ sản xuất đồng thời tối thiểu hóa rủi ro. Chúng tôi đã làm việc với nhiều loại hình khác nhau như vắc xin tiểu đơn vị tái tổ hợp, peptit, hormone, cytokine, yếu tố tăng trưởng, kháng thể đơn miền, enzym, plasmid DNA, mRNA và các loại khác. Chúng tôi chuyên về một số vi sinh vật như nấm men, tiết kiệm ngoài tế bào và trong tế bào (lượng thu lên đến 15g/L), vi khuẩn, tan trong tế bào và khối bao gồm (lượng thu lên đến 10g/L). Chúng tôi cũng đã tạo ra hệ thống lên men BSL-2 để tạo ra thử nghiệm phát hành lô Protein Tái Tổ Hợp và vắc xin. Chúng tôi là chuyên gia trong việc tối ưu hóa quy trình sản xuất, tăng năng suất và giảm chi phí. Chúng tôi có một đội ngũ công nghệ hiệu quả cao đảm bảo giao dự án đúng thời hạn và chất lượng tốt nhất. Điều này cho phép chúng tôi mang sản phẩm độc đáo của bạn ra thị trường nhanh hơn.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN