Chuyên môn cao và kinh nghiệm phong phú
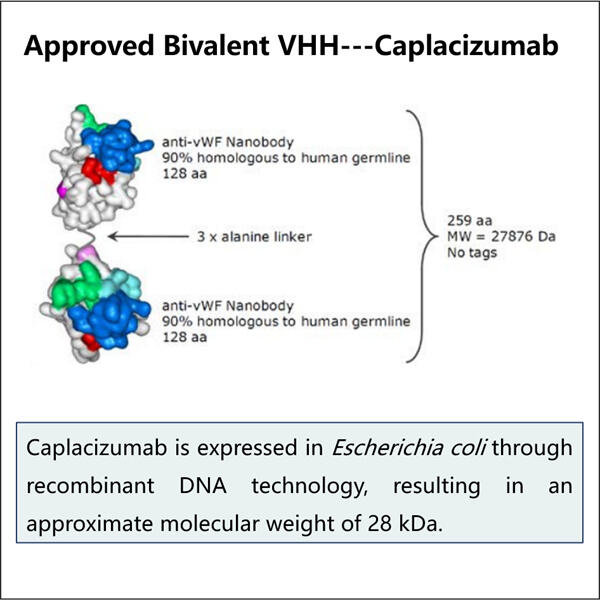
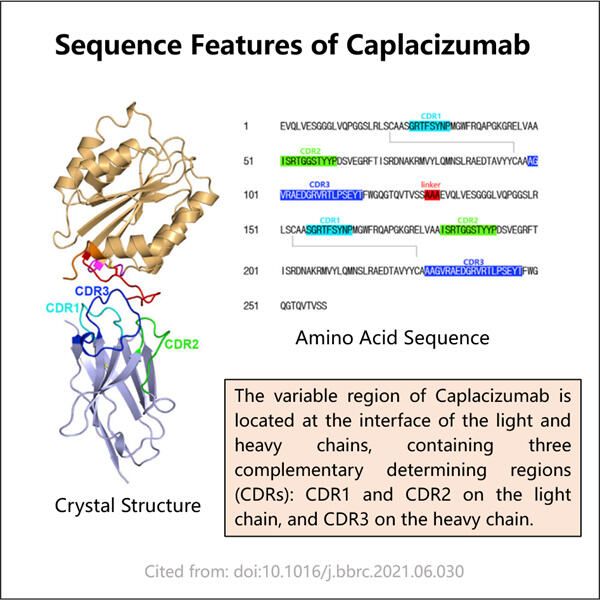
Yaohai Bio-Pharma là một CDMO vi sinh hàng đầu. Chúng tôi tập trung vào việc sản xuất Caplacizumab bằng phương pháp vi sinh và vắc xin cho con người, thú y và quản lý sức khỏe thú cưng. Chúng tôi có các nền tảng R&D hiện đại và phương pháp sản xuất bao gồm toàn bộ quy trình từ việc tạo chủng vi sinh, ngân hàng tế bào, phát triển quy trình và phương pháp đến sản xuất lâm sàng và thương mại cũng như thực hiện các giải pháp tiên tiến. Trong nhiều năm, chúng tôi đã tích lũy được nhiều kinh nghiệm trong xử lý sinh học sử dụng nguồn vi sinh. Chúng tôi đã thành công trong việc hoàn thành hơn 200 dự án trên toàn thế giới và đã hỗ trợ khách hàng điều hướng các quy định từ US FDA, EU EMA, Australia TGA và China NMPA. Với kiến thức và chuyên môn của mình, chúng tôi có thể phản ứng nhanh chóng với yêu cầu thị trường và cung cấp dịch vụ CDMO tùy chỉnh.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN