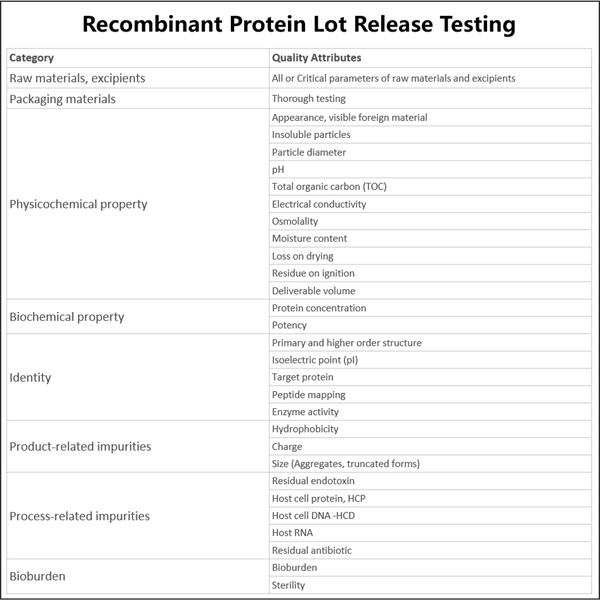
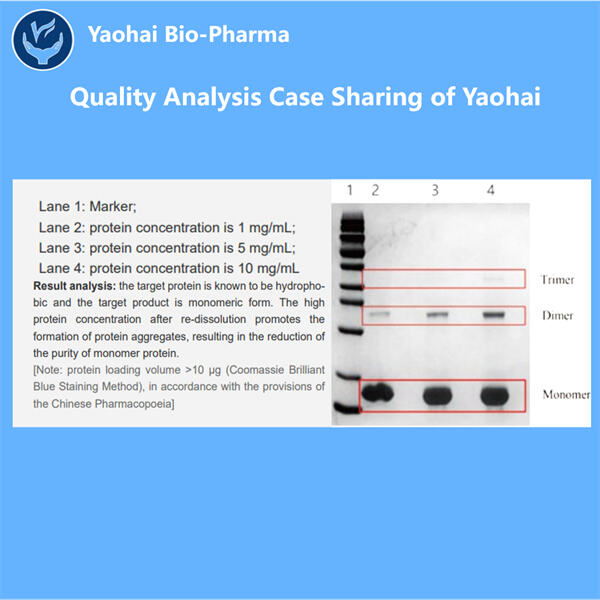
Aanpassing, Efficiëntie & Kosteneffectiviteit
Yaohai Bio-Pharma heeft ervaring in de productie van biologische middelen gemaakt uit microorganismen. We bieden maatwerk RD-oplossingen en productieservices terwijl we het risico minimaliseren. We hebben gewerkt met verschillende modaliteiten zoals recombinante subeenheid vaccins, peptiden, hormonen, cytokines, groeifactoren, mono-domein antilichamen, enzymen, plasmid DNA, mRNA en andere. We hebben gespecialiseerd in verschillende microorganismen zoals gist extracellulair en intracellulair afgeven (opbrengsten tot 15g/L), bacteriën intracellulair oplosbaar en inclusie lichamen (opbrengsten tot 10g/L). We hebben ook een BSL-2 fermentatiesysteem ontwikkeld om Recombinant Protein Lot Release Testing vaccins te creëren. We zijn experts in het optimaliseren van productieprocessen, verhogen van opbrengsten en verlagen van kosten. We beschikken over een zeer efficiënt technisch team dat zorgt voor punctueel en topkwalitatief projectaflevering. Dit stelt ons in staat uw unieke producten sneller op de markt te brengen.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN