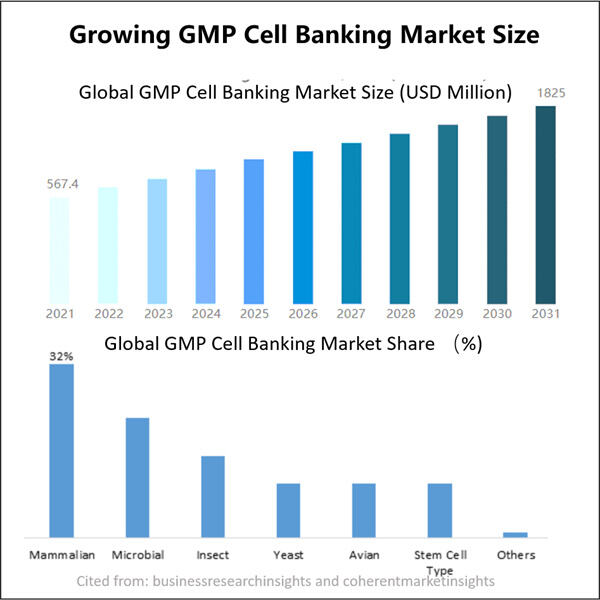
Fordelene ved GMP Mikrobielt Cellebank for Biopharmaceutisk Udvikling
Hvad får jeg ved GMP Mikrobiologisk Cellobank og at bruge den til at lave mit medicin? Dette vil effektivt spare nogen produktionstid, hvilket er en af de vigtigste fordele, da det kan verificere, om cellerne er konsistente over flere produktioner. Dette svarer til konsistent cellekvalitet, batch efter batch inden for samme batteri. Kvalitetskontrol - er vigtig, således at behandlingen faktisk følger dig hjem sikkert. Med en cellobank klar til brug, kan medicinalprodcenterne skabe en ny batch næsten så snart de mangler på deres sidste. Dette er for at sikre, at der er en god og regelmæssig lagerbeholdning af medicin.
Virksomheden skal sikre en patentprocedure og opretholde sine celler i en GMP CMV Antigen Produktion . Disse celler, der skal bruges til fremstilling af medicin, skal beskyttes mod tandkryd og andre forureninger. Det betyder, at ting som celler vokser i et rent og steril miljø. Det betyder også, at deres miljø er rent og fri for eventuelle kontaminanter, ikke sandt? Cellerne kryopreserves til transport og bevarelse ved meget lave temperaturer. Celleværelset skal også sikre, at mens cellerne bevares, kommer intet skadeligt (som bakterier eller virus, der kan være farlige) i dem. At tage sådan en omhyggelighed indebærer at sikre, at cellerne både er rene og klar til brug.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN